METAL KAPLAMA İLE İLGİLİ GENEL BİLGİLER
Tarihçe
Elektrolitik yolla metal kaplamacılığı 1843 yılında başlar. R. Boettper ilk nikel kaplamayı yapar. Banyo terkibi nikel sülfat ve amonyum sülfattır. 1849' da ilk olarak ticari anlamda nikel kaplamacılığı başlar. Gittikçe yeni terkipler geliştirilir. Karbonlu anotlar kullanılmaya başlanır. 1912' de İngiltere' de ilk parlatıcı kullanılır. 1915' ten sonra gelişmeler hızla artar. Watt's ve De Verter özellikle kaplamanın kalite kontrolü üzerinde durdular. 1935' te Thompson pH kontrolünün önemini belirtti. Modern parlak nikel banyolarının ticari anlamda değer kazanması ve kullanılmasını Schlötter başlattı. Daha sonra birçok gelişmeler oldu. İlk krom kaplamayı 1843' te Antoine Clesar Becquerel uyguladı. Kitabında krom klorür (CrCl3) ve krom sülfat Cr2(SO4)3 kullandığını belirtmektedir. Kromik asit çözeltisinden ilk krom kaplama 1856' da Geuther tarafından yapıldı. 1919 – 1924 yıllarında Sargeut çok çalıştı ve kromik asit çözeltisinin pratik ve uygunluğunu kitabında belirtti.
Genel Bilgiler
Elektrolitik olarak metalik bir eşyanın başka bir metal tabakasıyla kaplanması şu amaçlarla yapılır :
1 - Korozyona karşı koruma dayanıklılığının artırılması,
2 - Dekoratif amaçlarla daha iyi bir görünüm,
3 - Aşınma ve yıpranmaya karşı dayanıklılığının artırılması
4 - Kalıpların ve piston yataklarının darbelere karşı dayanıklılığın artırılması için.
Diğer bir metal kaplama şekli de ergimiş çinko içerisinde daldırma yolu ile yapılan galvanizlemedir. Konumuz elektrolitik yol ve doğru akımla yapılan kaplamadır. Bu usül de temel metale tutunma ve dayanıklılık bakımından en tercih edilenidir. Bu teknik bugün o kadar ilerlemiştir ki ABS (Akrilnitril – Butadion – Stirol) cinsi plastiklerin (ki bunlar iletken değillerdir) bazı ön işlemlerden sonra iletken hale getirilerek istenilen kaplamalarla (bakır, nikel, krom, altın, sarı ve gümüş) kaplanmaları kabil olmaktadır. Bu kaplama cinsleri sadece dekoratif amaçlı ve ince kaplamalardır. Kaplanacak parçalar radyo, televizyon düğmeleri, küçük panolar ve bijuteride kullanılan parçalardır. Bu plastikler enjeksiyon makinelerinde şekillendirildikten sonra iletken hale getirilerek istenilen kaplama yapılabilir.
Prensip
Bir metal yüzeyinin elektrolitik olarak kaplanmasında, yüzeyi kaplanacak olan cisim uygun bir elektrolite batırılır ve katot olarak kullanılır. Anot ise çöken metalden (kaplama cinsine göre çinko, bakır, nikel, kalay vs.) ve yüksek safiyette (%99.998) olmalıdır. Krom kaplamada ise çözünmeyen kurşun anot (%7 Sn+%93 Pb) kullanılır. Elektrolitik yolla kaplamada kullanılan akım doğru akım olup düşük voltajlıdır. Redresörlerden yararlanılır. Redresörlerin uygulama şekli 10 – 20 V ve 1200 – 2500 A verecek şekilde ayarlanır. Kademeli değil, değişken (variabl) redresörler tercih edilmelidir.
Elektrolitik olarak elde edilen bir metal tabakasını biçim ve yapısı yalnız metal cinsine değil, elektroliz koşullarına da bağlıdır. Bununla beraber işleme etki eden çeşitli yapıda tabakalar elde edilebilir. Bugün gerek metalografik, gerek X ışınları düfraksion yöntemleriyle metallerin kristal bir yapıda olduklan saptanmıştır. Buna göre katodda bir metalin çökmesi bir kristalleşme olarak düşünülebilir. çözüntünün özellikleri kristalin yapısına ve büyüklüğüne bağlıdır. Kristallerin oluşma biçimi iki etkene bağlıdır :
- Kristallerin oluşum hızı,
- Kristallerin gelişme hızı.
Eğer kristal zerrelerin büyüme hızları bunların oluşum hızından çok daha büyük ise çöküntü büyük kristaller halinde, aksi halde küçük kristaller halinde olur. Demek oluyor ki zerrelerin oluşumunu kolaylaştıran koşullarda, küçük kristaller meydana gelir, küçük kristalli yapı gayet düzgün ince ve yapışık bir tabaka sağlar.
Kaplamada İzlenen Aşamalar
Süngerli, poröz (zamak gibi) yapılarda kristaller arasında hidrojen (H2) gazının yerleşmiş olmasından dolayı az yapışık özelliktedir, zamanla kabarmalar yapar. Onun için katotta hidrojen çıkışını önlemek gerekir. Temel metale iyi yapışık ve dayanıklı bir tabakanın elde edilmesinde en başta gelen en önemli faktör kaplanacak parçanın yüzeyinin temizliğidir. Kaplanacak parçaların, kaplama banyolarına girmeden önce tabi tutulacağı işlemler çok mühimdir. Kaplanacak yüzeyin temizliği noksan ise yapılan tüm çalışmalar boşunadır. Malzeme, zaman ve enerji kaybına sebep olur.
Bir kaplama işlemi genel olarak
- Elektrolitik yolla kaplama olmak üzere iki kısımda incelenebilir.
Polisaj işlemi tek motorlu sistemlerden tam otomatik sürekli sistemlere (band polisajı) geçmiş büyük bir aşama göstermiştir. Zamak, pirinç (sarı) parçaların önce çelik telden fırçalarla çapakları alınır. Ayrıca özel keçe ve özel cilalarla kumaştan veya sisal fırçalarla parlatılmaları sağlanır. Kaplanacak yüzeyler bir ayna parlaklığına getirilir. Burada en önemli husus ; demir, zamak veya aluminyum parçaların polisajlarının birlikte ve aynı polisaj tezgahında değil, ayrı ayrı tezgahlarda yapılmasıdır. Birlikte ve aynı tezgahta yapılan polisajda aluminyum tozları yangına sebep olur. Zamak döküm parçalarda, döküm hatalarından ileri gelen, gözle görülemeyen süngerimsi poröz oluşumdan dolayı boşluklarda hava veya kimyasal atık kalması nedeniyle kaplamadan sonra bu yerlerde kabarmalar olur. Bu kabarmaların bir önemli sebebi de zamak döküm işlerinde yolluk adı verilen parçaların hurda malzeme ile orijinal malzemeye fazla katılmasından doğar.
Yüzey Temizleme
Yağ, Cila Artıklarından Temizleme :
Yüzeyi yağ ve cila artıklarından organik yağlardan oluşan kirlilik alkalik sıcak yağlama banyolarında sabunlaştırma ile giderilebilir. Hazır terkipler (ilaçlar) % 5 – 10 oranında suda eritilerek 65 – 70 °C' de 15 – 20 dakika müddet ile işleme tabi tutulurlar. Terkipte ekseriya "sudkostik, soda, trisodyum fosfat" ile inhibitör veya emülgatör yardımcı kimyasallar bulunur. Bunlar da temel metalin cinsine göre Alzamak, sarı pirinç ve demir için değişik oranlardadır.
Keza elektrolitik yağ almada da bu maddelerle birlikte bazı ilave tuzlar kullanılmak suretiyle, normal sıcaklıkta anodik veya katodik çalışılarak birkaç dakika gibi zaman diliminde işleme tabi tutulur. Katotta çıkan hidrojen gazı miktarı anotta çıkan oksijen gazının iki katı olduğundan gazın temizleme etkisi katotta daha fazladır. Mineral yağlar sabunlaşmazlar, bu tür yağlar ultrasonik temizleme ile giderilmelidir. Eskiden triklor etilen veya perklor etilen ile buhar fazında temizleniyor idi.
Elektrolitik yolla metal kaplamacılığında sıcak yağ alma, elektrolitik yağ alma ve müteakip işlerin peşpeşe hiç ara verilmeden yapılması gerekir.
Parça Yüzeyindeki Oksit ve Pasın Giderilmesi :
Demir ve çelikten imal edilmiş parçaların yüzeyindeki oksit ve pasın giderilmesi için tuz ruhu, sülfürik asit tek başına veya her ikisinin karışımı muhtelif konsantrasyonlarda, maliyetlerinin düşük olması avantajı ile kullanılmakta iseler de dezavantajları daha fazladır. Malzeme sathında pas giderildikten sonra bekleme süreci içerisinde malzeme tekrar paslanabilmektedir. Yüzey tekrar kararmakta, aşınmakta ve bazen de lekeler oluşmaktadır. Ayrıca atölyeler ve çalışma yerlerinin çok iyi aspirasyonu (havalandınlması) gerekmektedir. Asit buharları diğer ham mamülleri ve civarda bulunan aparat ve cihazlan korozif etkisi dolayısıyla paslandıracaktır.
Pas ve kireç çözücüsü, yüksek kesafeti, etkin pas alıcı ve kireç sökücü özelliğiyle, temel metale etki vermeyen özelliğiyle geniş bir kullanım alanını kapsar. Yukarıda adı geçen asitleri içermez, aspirasyon gerektirmez ve hiçbir korozif etkisi yoktur. Parça yüzeyinde kaynak ve lehimleme sonucu oluşan pisliklerin giderilmesinde de pas ve kireç sökücü kullanılmaktadır. Adı geçen ürün elektrokimya sanayiinin imalatıdır.
Elektrolitik ve Kimyasal Parlatma
a- Elektrolitik Parlatmada Prensip : Metal, elektrolitik bir pilde anot olarak kullanılır. Metalin çözünmesi o şekilde olur ki, yüzeydeki pürüzler kalkar ve yüzey düz ve parlak olur. Elektrolitik parlatma işlemi her metal için özel terkiplerde (özel banyolarda) yapılır.
Özetle: Özel banyolarda metali anodik çözündürmeye uğratmak ve yüzeyinin parlatılmasını sağlamaktır.
b- Kimyasal Parlatma : Dışarıdan bir potansiyel uygulamadan, metali kendisini çözen bir banyoya daldırıp kimyasal çözünmeye uğratarak yüzeyinin düzeltilip parlatılmasıdır. Reaksiyonun yürüyüşü elektrolitik parlatmaya benzer, tek farkı burada iki ayrı elektrot (anot ve katot) olmayıp, anot ve katot olarak oluşmakta ve anodik bölgeler film yardımıyla aşınmaktadır. Yani kısaca yüzeyde oluşan lokal piller olaya yön vermektedir.
Banyolarda Kaplama
Polisajı icabeden parçalar polisaj işleminden sonra bekletilmez. Parçaların ciladan oluşan yağlı kirliliği yukarıda belirtildiği gibi sıcak alkali ve elektrolitik yağ alma işlemlerine tabi tutulur. Parçalar elektrolite daldırılır ve akım verilir, bazı durumlarda da parçalar akım altında asılır. Aksi halde metal yüzeyinde bir oksit tabakası oluşur. Kaplama işleminin aralıksız devam etmesi gereklidir. Birbirini takip eden kaplama banyolarında da parçalar havada bekletilmemelidir. Akım kesilmesi gibi durumlarda ise son kaplanmış veya yarı kaplanmış parçalar bir sonraki yıkama banyosunda bekletilmelidir. En son kaplamadan çıkan parçalar (kaplama işlemi biten parçalar) demineralize sıcak suda 95 °C' de 5 – 10 dakika bekletilir. İşlem tamamlanır. Misal olarak ;
Parlak dekoratif bir krom kaplamada işlem sırası şöyle olmalıdır :
- Sıcak alkali yağ banyosunda yağdan giderme.
- Su ile yıkama, çalkalama.
- Elektrolitik yolla yağdan giderme. (Anodik veya katodik)
- Su ile yıkama, çalkalama.
- Nötralizasyon. (demir malzeme için %8 – 10 H2SO4 , zamak malzeme için %5 H2SO4 + %1 – 2 HF)
- Su ile yıkama, çalkalama.
- Ön siyanürleme (%3 – 5 NaCN). Parçalar daldırılıp çıkarılır.
- Siyanürlü bakır kaplama (5 sn. anodik 25 sn. katodik) tavsiye edilir.
- Ekonomik yıkama. (Bu asla dökülmez ve arıtmaya verilmez)
- Su ile yıkama, çalkalama. (Kaskatlı)
- Nötrleme (%5 – 10 H2SO4 ile)
- Su ile yıkama, çalkalama.
- Parlak nikel kaplama. (Bazı özel durumlarda dublex nikel kaplama tatbik edilmektedir)
- Ekonomik yıkama. (Bu asla dökülmez ve arıtmaya verilmez.)
- Su ile yıkama, çalkalama.
- Parlak dekoratif krom kaplama.
- Ekonomik yıkama. (Bu asla dökülmez ve arıtmaya verilmez.)
- Su ile yıkama, çalkalama, durulama.
- Demineralize 95 °C sıcak suda sealing ve kurutma.
Not : Ekonomik yıkama banyoları çıktıkları banyonun elektrolitlerini ihtiva ederler. Mesela, nikel kaplamadan sonraki ekonomik yıkama nikel iyonlarıyla, yardımcı katkı maddelerini içerir, nikel banyosuna yapılacak takviyelerde bu yıkama suyu kullanılır. Ayrıca tüm ekonomik yıkama banyoları deiyonize su ile hazırlanmalıdır.
GENEL TARİFLER
1. KESAFET (yoğunluk – dansite – özgül ağırlık) : Bir cismin 1 ml. sinde (1 cm3 ünde) bulunan çökelti kütlesidir. (d) ile gösterilir.
çökelti kütlesi (gr.)
d = = . . . gr /ml
çökelti hacmi (ml.)
Her elementin yoğunluğu ayrı ayrıdır.
Su 1 gr /ml. Cr 7,20 gr /ml.
Al 2,7 gr /ml. Cu 8,96 gr /ml.
Fe 7,8 gr /ml. Ni 8,90 gr /ml.
Zn 7,1 gr /ml. Pb 11,35 gr /ml.
Sn 7,3 gr /ml. Hg 13,60 gr /ml.
2. YÜZDE (%) : Bir çözeltinin 100 gramında bulunan çözünmüş maddenin kütlesidir.
gram
Yüzde (%) =
100 gr.
Mesela : % 15 lik bir sudkostik çözeltisi ne demektir?
15 gr. sudkostiğin 85 ml. sudaki çözeltisidir. (suyun yoğunluğu 1 dir.) Toplam 100 gramdır.
NOT : % 96 lık bir sülfürik asitten %30 luk bir sülfürik asit çözeltisi hazırlanacak ise burada çapraz kaide yönteminden yararlanılılr. Şöyle ki ;
Sülfürik asit 96 30 Alınacak asit miktarı
30
Su 0 66 Alınacak su miktarı
%96 lık asit % 30 asit farkı 66 dır. 66 k su alınacaktır. Su % 0 hazırlanacak % 30 farkı 30 olup 30 k. asit alınacaktır.
Karışımın % si 30 dur. Karışımı hazırlarken ASLA asit üzerine su dökülmez. Suyun üzerine yavaş yavaş ve kabın cidarından azar azar asit ilave edilmelidir.
3. KONSANTRASYON : Çözeltinin 100 ml.sinde bulunan çözünmüş maddenin kütlesidir.
gram
konsantrasyon =
100 ml.
Konsantrasyonu 20 olan bir çözelti demek ; 20 gram madde 100 ml. çözücüde çözünmüş demektir.
4. ELEKTROLİT : Elektroliz kabında (+) pozitif kutup ANOT, (–) negatif kutup KATOT adını alır. Elektrik akımını geçiren maddelere İLETKEN, elektrik akımını geçirmeyen maddelere YALITKAN adı verilir. Anoda giden (–) negatif yüklü iyonlara ANYON , katoda giden (+) pozitif yüklü iyonlara da KATYON adı verilir.
5. ELEKTROLİZ : İyonlara ayrılabilen bir cismin sulu çözeltisinde, su dipollerinden ibaret bir cins bulutla çevrili, yani hidratize olmuş (+) ve (–) yüklü iyonlar vardır.
Bir bakır klorür (CuCl2) çözeltisinde sudaki (H+) ve (OH-) iyonlarının yanında (Cu+) ve (Cl-) iyonları bulunur. Bu çözeltiye iki platin levha sokup bir doğru akım kaynağının iki farklı kutbuna bağlayıp akım geçirirsek :
(+) yüklü (Cu++) iyonları negatif elektroda KATOD'a gider. (-) yüklü (Cl-) iyonları ise pozitif yüklü eletroda ANOD'a gider.
Cu++ iyonları katotta elektrik yüklerini bırakırlar. Her bakır iyonu elektrottan iki elektron alır, böylece Cl- iyonları elektrikçe nötral olan klor gazı haline geçerler.
2 Cl- iyonu ® 2 Cl atomu ® Cl2 molekülü
Bir atom-gram bakırın elektrotta açığa çıkarılması için 2 x 96.490 (coulomb) gerekir.
Elektrolitik kaplamanın "Galvanoteknik" yani metal kaplamacılığının temelini işte bu elektroliz olayı oluşturur.
ELEKTROLİZ OLAYINA ÖRNEKLER
A – (Çözünmeyen Pt elektrot ile) Sülfürik Asit çözeltisinin elektrolizi (Şematik) :
| 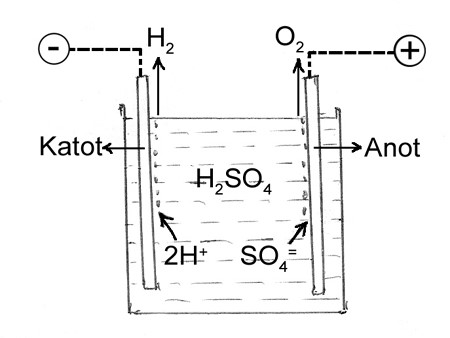
| Katotta : 2H+ + 2 é ® H2& Anotta : SO4= – 2 é ® SO4 (doymamış molekül grupları) SO4 + H2O ® H2SO4 + ½ O2& (H2SO4 + O) H2SO4 ® 2H+ + SO4= |
B – (Çözünmeyen Pt elektrot ile) Bakır Sülfat çözeltisinin elektrolizi :
| 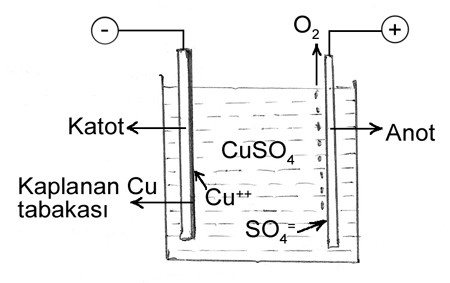
| Katotta : Cu++ + 2 é ® Cu (katotta toplanır, Cu kaplama) Anotta : SO4= – 2 é ® SO4 (doymamış molekül grupları) SO4 + H2O ® H2SO4 + ½ O2 & (H2SO4 + O) H2SO4 ® 2H+ + SO4= |
C – (Çözünen bakır anot ile) Bakır Sülfat çözeltisinin elektrolizi :
| 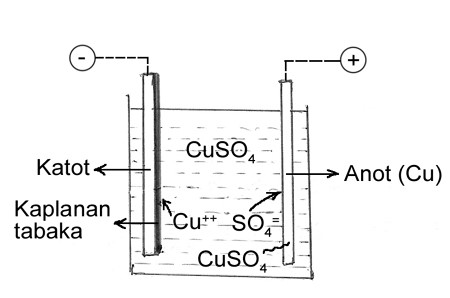
| Katotta : Cu++ + 2 é ® Cu (katot yüzeyinde toplanır) Anotta : SO4= – 2 é ® SO4 (doymamış molekül grupları) SO4 + Cu ® CuSO4 CuSO4 ® Cu++ + SO4= (elektrolitteki Cu++ miktarı çözünen Cu anottan dolayı eksilmez, sabit kalır) |
6. OHM KANUNU : 1 Ohm (W) ; içinden 1 Amper' lik akım geçtiğinde iki nokta arasında 1 Volt' luk potansiye1 farkı gösteren bir iletkenin bu iki nokta arasındaki direncidir.
7. DİRENÇ : Bir iletkenin direnci onun boyu (l) ile doğru orantılı, kesiti (s) ile ters orantılıdır. Direnç (R) ile gösterilir.
l
R = g . (g) katsayısına özgül direnç denir.
s
8. VOLT : 1 Ohm'luk bir dirençten 1 Amper geçiren kuvvettir.
9. AMPER : Akım şiddeti birimidir. Bir iletkenden zaman biriminde geçen elektrik miktarıdır. Yani 1 Amper bir iletkenden 1 Saniyede 1 Coulomb geçirilmesiyle elde edilir.
10. 1 COULOMB : Bir gümüş nitrat çözeltisinden 1,118 mg. gümüş açığa çıkaran elektrik miktarı 1 coulomb (kulon)' dur.
11. FARADAY KANUNU : Herhangi bir iyonun 1 ekvivalent gramının nötr element haline geçebilmesi için daima aynı miktarda. yani 96.490 coulomb'a ihtiyacı vardır. Yani elektrolizde elektrolitin 1 ekvivalent gramını açığa çıkaran elektrik miktarıdır. Bu da 96.490 coulomb'dur ve elektronun yükü ile Avagadro sayısının çarpımına eşittir.
Faraday (F) = 96.490 coulomb veya
(F) = 96.490 Amper-saniye veya
(F) = 26,801 Amper-saat
1 coulomb = 1 Amper-saniye
1 c = 1 As
1 saat = 3.600 saniye
1 Ekvivalent eşdeğer = 96.490 /3.600 = 26,8 Ah
Galvanoteknikte amper-saat geçerlidir.
1 Amper-saatte ayrılan metal miktarı (e) elektrokimyasal eşdeğer olarak bilinir.
Atom ağırlığı
c = ekvivalent eşdeğer gr (gr /Ah)
Değerlik x 26,8
Örnek : Gümüş'ün eşdeğer miktarı nedir?
Çözüm : Ag atom ağırlığı 108
değerliği 1
108
c = = 4,03 gr /Ah
1 x 26,8
Örnek : (+6) değerlikli Krom'un eşdeğer miktarı nedir?
Çözüm : Cr atom ağırlığı 52
değerliği 6
52
c = = 0,323 gr /Ah
6 x 26,8
Örnekler :
+2 değerlikli Ni++ eşdeğer miktarı c = 1,095 gr /Ah
+3 değerlikli Al+++ eşdeğer miktarı c = 0,355 gr /Ah
+2 değerlikli Zn++ eşdeğer miktarı c = 1,220 gr /Ah
+1 değerlikli Au+ eşdeğer miktarı c = 7,357 gr /Ah
12. AKIM YOĞUNLUĞU : Galvanoteknikte akım şiddetinin yerine, elektrotların birim yüzeyine isabet eden akım şiddeti alınır. Buna akım yoğunluğu denir. Birim yüzey dm2 dir.
i (amper)
d = = . . . [A / dm²]
s (dm²)
13. pH NEDİR? pH değeri H+ iyonları molar konsantrasyonu olarak tarif edilir.
H2O ® H+ + OH- . . . . . (1)
Kütlelerin tesiri kanununa göre :
[H+] [OH-]
= K = 1,7 x 10-16 . . . . . (2)
(H2O)
Suyun molar konsantrasyonu 55 sabit olarak kabul edilebilir, yani :
[H+] [OH-] = K = 10-14 . . . . . (3)
Bu K sabitesine suyun "iyonizasyon" veya "dissosiasyon" sabitesi denir. Bu da elektriksel metodlarla ölçülmüş ve 22 °C' de K = 10-14 bulunmuştur.
Bu yalnız saf su için değil, asidik, alkali ve bütün sulu çözeltiler için gereklidir. Saf suda ve nötral çözeltilerde H+ ve OH- birbirine eşit olduğundan her birisi; 10-7 dir. Yani :
pH = – log [H+]
pOH = [OH-]
pH + pOH = 14 tür.
Buna göre çözeltileri şöyle sınıflandırmak kabildir :
pH = pOH = 7
pH = 7 nötral çözelti
pH < 7 < pOH asidik çözelti
pH > 7 > pOH alkali çözelti
Sorensen, logaritmik ifadeler yerine, yani H+ iyonları konsantrasyonu 10-7 dir demek yerine, pH 7 dir demeyi uygun görmüştür.
NOT : pH değerlerini hassas 0,5 – 5,5 / 5,5 – 9,0 / 9,0 – 14,0 aralıklı pH kağıtları ile ölçebileceğiniz gibi, en iyisi pH metre cihazı ile ölçmektir.
14. ELEKTROLİTİK KAPLAMANIN ÜZERİNE TESİR EDEN FAKTÖRLER :
a. Akım yoğunluğu,
b. Konsantrasyon (banyo terkibi) ve karıştırma,
c. Sıcaklık (elektrolitin temperatürü)
d. Temel metalin ve elektrolitin tabiatı.
e. pH değeri,
f. Dağılma gücü (kaplama gücü)
15. °BAUME (BOME) DERECESİ (°Bé) – ARCOMETRE DERECESİ :
Bu derecenin tayininde sudan hafif ve sudan ağır sıvılar için iki tip arcometre kullanılır.
a. Sudan ağır sıvılarda kullanılacak arcometre % 10' luk tuzlu suya daldırıldığı zaman görülen nokta 10 (on), saf (destile) suda görülen nokta 0 (sıfır) olarak işaretlenir ve on parçaya bölünür.
b. Sudan hafif sıvılarda ise ayar tamamen yukarıdakinin aksidir. Yani % 10 luk tuzlu suya batan kısım 0 (sıfır), saf (destile) suda görülen kısım 10 (on) olarak alınmıştır. Yine aralık on eşit parçaya bölünür.
Yoğunluk (dansite) ve °Baume Derecesi Arasındaki İlgi :
a. Sudan ağır sıvılar için :
144,32
d =
144,32 – °Be
b. Sudan hafif sıvılar için :
144,32
d =
144,32 + (°Be – 10)
MÜHİM NOT : Metal kaplamacılığında elektrolitlerin °baume derecelerine göre banyo takviyeleri yapmak doğru değildir. °Baume derecesi daima yanıltır. Analiz değerlerine itibar edilmelidir.
16. ÇEŞİTLİ METALLERİN EBATLARINA GÖRE ANOT' LARIN AĞIRLIKLARI:
| Anot Cinsi | Yoğunluk | Kalınlık | 300 x 200 | 400 x 200 | 500 x 200 | 600 x 200 |
| Saf Kurşun | 11,34 | 5,0 mm. | 3,400 kg. | 4,540 kg. | 5,670 kg. | 6,800 kg. |
| Kadmiyum | 8,64 | 6,0 mm. | 3,110 kg. | 4,150 kg. | 5,180 kg. | 6,220 kg. |
| Bakır | 8,93 | 5,0 mm. | 2,680 kg. | 3,570 kg. | 4,470 kg. | 5,360 kg. |
| Sarı M63 | 8,55 | 5,0 mm. | 2,570 kg. | 3,420 kg. | 4,280 kg. | 5,130 kg. |
| Nikel | 8,85 | 8,0 mm. | 4,250 kg. | 5,660 kg. | 7,080 kg. | 8,500 kg. |
| Çinko | 7,14 | 5,0 mm. | 2,180 kg. | 2,910 kg. | 3,640 kg. | 4,370 kg. |
| Kalay | 7,28 | 5,0 mm. | 2,140 kg. | 2,860 kg. | 3,570 kg. | 4,280 kg. |
| Altın | 19,30 | 0,7 mm. | 20 mm. genişlik 1 mt. levha 270 gr. |
| Gümüş | 10,50 | 2,0 mm. | 400 x 250 mm. 1 mt. levha 2,100 kg. |
| | | 3,0 mm. | 400 x 250 mm. 1 mt. levha 3,150 kg. |
| | | 5,0 mm. | 400 x 250 mm. 1 mt. levha 5,250 kg. |
17- GALVANOTEKNİKTE "FAYDALANILABİLEN AKIM NİSBETİ" :
Kaplamacılıkta doğru akım kaynağı "redresör"ün gösterdiği amper, kaplama cinsine göre vereceğimiz akım yoğunluğunun biraz üzerinde tutulmalıdır. Şöyle ki :
1,5 A /dm² akım yoğunluğuyla ve toplam 180 A tutan redresör ampermetresinin 190 – 200 A göstermesi sağlanmalıdır. Direnç ve baralardaki akım kayıpları da nazari itibara alınmalıdır. Bazı kaplama cinslerinin faydalanılabilen akım yüzdeleri şöyledir :
Parlak dekoratif nikel % 95 – 98
Parlak gümüş % 98
Bakır (asitli) % 98 – 100
Bakır (siyanürlü) % 80 – 90
Bronz % 95 – 100
Çinko (siyanürlü) % 75 – 95
Çinko (asitli) % 95 – 100
Kalay (alkali) % 85 – 98
Krom (sülfürik asitli) % 10 – 12
Krom (katalistli) % 27
Kurşun % 90 – 100
Sarı (pirinç) % 75 – 80
18- Aydınlatma sanayii için yapılan reflektör vs.nin ışığı yansıtma ölçümlerinin yüzdeleri de şöyledir :
(ortalama değerler)
Gümüş için % 88
Aluminyum için % 85
Kalay için % 70
Krom için % 66
Nikel için % 55
Bakır için % 62
Altın için % 61
Kadmiyum için % 52
Çinko için % 50